
強心苷甾體是廣泛分布于自然界的一類特殊的代謝産物家族,其結構的甾體骨架中往往含有一個特征的C14β-OH,C17位由五元或六元不飽和内酯環連接(代表了兩類強心苷結構類型),同時C3位可能存在糖單元修飾。植物産生的強心苷分子往往C17位包含有一個γ-丁内酯環;而兩栖動物,如蟾蜍中産生的強心苷C17位則為δ-戊内酯單元(圖1)。多年來該類分子主要用作強心劑,随着強心苷分子的抗腫瘤、抗炎、抗病毒等活性的開發,豐富且良好的生物活性使其目前活躍于多項臨床研究中。然而,目前工業生産該類藥物仍然采取從動植物中原位提純的方式,這嚴重限制了強心苷分子的應用;此外強心苷結構上的微小差異極大地影響了其生理活性。因此越來越多的研究緻力于探索和解析強心苷複雜結構的生物和化學合成過程,為其更高效地工業量産提供新的思路。

圖1 強心苷明星分子
2022年7月28日,ACS Catalysis期刊在線發表了戈惠明團隊關于強心苷甾體的最新研究成果。通過生物催化甾體小分子雄烯二酮的C14位發生惰性C-H鍵的活化,再聯合化學手段構造一條高效的合成途徑,并成功運用于兩類強心苷天然産物—bufotalin, bufogenin B, digitoxigenin的合成。

圖2 生物和化學催化的強心苷分子的交叉合成策略
在前人的研究中,強心苷分子的生物合成主要集中于由膽固醇前體代謝形成孕酮等甾體中間體的過程,對于特征的C14位羟基化以及C17位的不飽和内酯環的組裝鮮有報道。因此,研究者針對該類分子特征的C14β-OH的形成展開研究,對可能催化羟基化的P450酶進行挖掘。首先選取能夠産生強心苷分子的植物牛角瓜為研究對象,對其不同組織的轉錄水平進行分析,最終通過篩選出候選的11個P450基因的功能驗證,并結合強心苷生物合成中間體—孕酮和其結構類似物雄烯二酮的飼喂,确定了CYP11411能夠催化甾體C14位産生α-OH,而該構型與目的構型相反。研究者對另一類強心苷産生宿主動物蟾蜍進行研究,發現CYP44476同樣能夠催化甾體小分子底物發生C14位的氧化羟基化,同時還能夠催化甾體的C6、C9、C15位形成羟基。根據動植物宿主中羟化酶的研究結果,推測自然界可能優先通過直接攫取α-H産生α-OH,再經過脫水水合等途徑完成構型的翻轉。
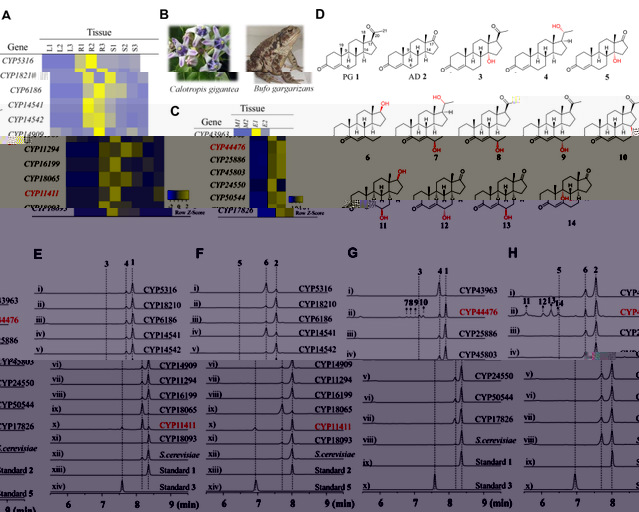
圖3植物牛角瓜及動物中華大蟾蜍的轉錄組分析、候選P450的功能驗證及代謝産物的結構
該團隊首次發現了強心苷産生宿主中的C14羟化酶,能夠直接實現惰性甾體骨架的位點特異性氧化,而這通過化學反應則難以一步完成。為了完成強心苷分子的合成,研究者拟通過生物催化完成C14羟基化甾體的大量合成,再經過化學手段組裝C17位的含氧雜環。因此,需要對C14羟基化甾體進行規模制備。通過對羟化酶的異源表達代謝譜分析發現其轉化效率較低,于是通過将目标轉至綠色高效地微生物生物轉化。通過對微生物菌株的篩選和羟基化活性測試,最終發現新月彎孢黴C.lunata能夠以較高效率催化生成目标産物(圖4),進一步優化後分離收率能夠達到70%,并獲得了5g的C14α-OH-雄烯二酮。
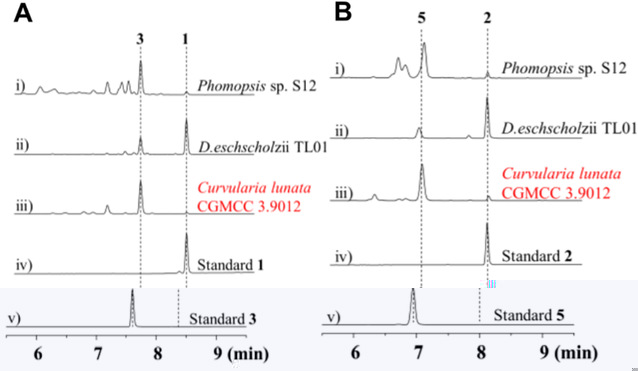
圖4微生物菌株的甾體C14位羟基化活性測試
接下來,研究者們着手于利用化學合成完成C17位五元或六元不飽和内酯環的組裝。首先,通過底物C14α-OH-雄烯二酮的∆4,5位氫化還原構建A/B cis環系,然後選擇性還原C3位羰基及羟基的矽醚保護獲得化合物17。為了實現關鍵C14位羟基構型的翻轉,先通過脫水消除α-OH,再經Mukaiyama水合産生β-OH産物。而在烯烴水化過程中,産物異構體比例與反應溶劑息息相關。由烯基碘中間體21出發,可分别偶聯五元或六元内酯環(圖5)。

圖5 底物14α-OH-雄烯二酮合成關鍵烯基碘化物中間體21
為了完成強心苷甾體的合成,通過化合物21與錫試劑的Stiile 偶聯反應構建了強心苷的基本骨架。∆16,17雙鍵能夠通過氧化形成三元氧環,經TMSOTf和2,6-lutidine催化形成C14矽醚而發生1,2-氫遷移實現開環重排。最終通過C16位羰基還原,乙酰化反應和保護基的脫除,成功獲得了天然産物bufotalin和bufogenin B(圖6)。

圖6 天然産物bufotalin和bufogenin B的合成路線
由化合物21形成的烷基碘化物則更易發生自由基反應。化合物33與馬來酸酐在自由基供體TTMSS和引發劑AIBN作用下完成類SN2自由基偶聯反應。随後,在堿性條件下,生成的C14位羟基參與形成内酯環。NaBH4-MeOH選擇性還原和内酯化(經曆開環再成環過程)形成35,苯基氯化硒衍生物進一步氧化獲得不飽和内酯環産物,酸水解後獲得最終産物digotoxigenin(圖7)。

圖7 天然産物digotoxigenin的合成路線
綜上,該團隊首次從強心苷天然産生宿主中鑒定出兩個能夠催化C14位羟基化的P450酶——CYP11411和CYP44476,為其生物合成途徑的闡釋打下基礎。同時通過微生物的高效轉化規模化合成了甾體C14α-OH-雄烯二酮,并以其為底物通過組裝不飽和内酯環單元完成了兩類強心苷天然産物的合成。這種利用生物催化和合成化學的方式開發通用且靈活的合成策略,可用于創制更多生物活性的強心苷分子及其結構類似物。
伟徳国际官网登录入口趙陽博士生為文章的第一作者,伟徳国际官网登录入口戈惠明教授、譚仁祥教授和化學化工學院俞壽雲教授為文章的通訊作者。該研究得到了國家重點研發計劃、國家自然基金委傑出青年基金、青年基金及中央高校基本科研業務費等項目的資助。
原文鍊接:https://doi.org/10.1021/acscatal.2c02185
文章題目:Biocatalytic C14-Hydroxylation on Androstenedione Enabled Modular Synthesis of Cardiotonic Steroids