癫痫是最常見的神經系統疾病之一,發病率接近1%,其中約30%的患者會發展為藥物難治性癫痫,尤其是伴有海馬硬化的颞葉性癫痫患者,此部分患者除手術外,治療方法十分有限。颞葉性癫痫患者緻痫區的兩大主要病理學特征是神經元死亡和膠質瘢痕的産生,膠質瘢痕的主要組成細胞是反應性星形膠質細胞。然而,在癫痫病理進程中,反應性星形膠質細胞的功能及其分子機制仍不清楚。
近日,我院闫超教授、陳迪俊教授聯合伟徳国际官网登录入口醫學院附屬鼓樓醫院神經外科劉翔宇主任,首次揭示了颞葉性癫痫患者的大腦中存在一種新的反應性星形膠質細胞亞群——脂質堆積的反應性星形膠質細胞(lipid-accumulated reactive astrocyte, 簡稱LARA);LARA以依賴APOE的方式形成,表現出獨特的分子表型和功能表型;LARA通過上調腺苷A2A受體表達,降低谷氨酸的重攝取,進而加劇神經元的興奮性,促進癫痫的疾病進展。該發現可以為治療耐藥性癫痫提供全新的策略。

研究人員首先通過分析颞葉性癫痫(temporal lobe epilepsy, TLE)患者的磁共振成像波譜數據,發現患者的緻痫側海馬中存在脂質異常堆積,進一步的免疫熒光和脂代謝組學實驗表明脂質堆積是TLE患者的重要病理特征,并且脂質堆積主要發生在神經元和星形膠質細胞中。進一步通過收集TLE患者腦組織樣本進行單核RNA測序發現,TLE患者中星形膠質細胞脂代謝和脂轉運信号通路異常激活,并且載脂蛋白APOE在星形膠質細胞中顯著上調。接下來研究者在癫痫小鼠模型中發現,星形膠質細胞特異性APOE敲除能有效改善星形膠質細胞中的異常脂堆積;體外細胞實驗結果也表明神經元過度興奮産生的大量脂質會被星形膠質細胞來源的APOE轉運到星形膠質細胞,導緻其異常脂堆積。研究人員發現,這些脂堆積異常的星形膠質細胞是一群新的反應性星形膠質細胞。根據單核RNA測序數據,他們鑒定出一個高表達APOE的星形膠質細胞亞群,并表征了其轉錄組特征,研究者将這個亞群定義為“脂堆積的反應性星形膠質細胞”,英文簡稱為LARA。
為了探究LARA在癫痫病理中的作用,研究人員對APOE敲除小鼠中進行癫痫造模,發現APOE敲除能有效改善癫痫症狀,也能逆轉絕大部分LARA相關基因的表達水平,表明APOE是LARA形成的必要條件,且LARA具有促癫痫的作用。最後,研究團隊還初步探索了LARA促癫痫的潛在分子機制,發現LARA通過上調腺苷A2A受體來發揮促癫痫作用。使用腺苷A2AR抑制劑或特異性敲低星形膠質細胞的腺苷A2A受體,都能夠改善模型小鼠的癫痫症狀。
綜上,這項研究發現TLE患者病竈區存在異常脂堆積現象,定義了一種全新的反應性星形膠質細胞亞型——LARA,并系統研究了LARA在TLE中的分子表型和功能表型,同時首次揭示了APOE在癫痫疾病進展中的作用,為治療耐藥性癫痫提供了全新的策略。
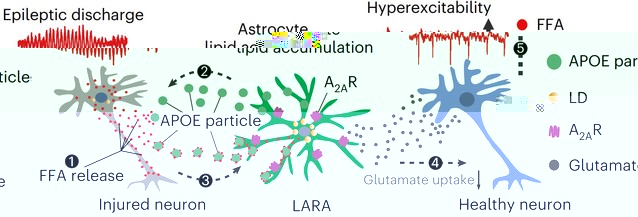
圖1. LARA的形成及其促進癫痫進展的原理示意圖
該研究成果以“Lipid-accumulated reactive astrocytes promote disease progression in epilepsy”為題,于2023年03月20日發表于神經科學領域頂級期刊Nature Neuroscience。我院闫超教授、醫學院附屬鼓樓醫院神經外科劉翔宇主任、我院陳迪俊教授為該論文的通訊作者;我院助理研究員陳張朋為第一作者兼通訊作者;我院博士生王素吉、趙賢森、方雯為共同第一作者。該工作得到國家自然科學基金等項目支持。
原文鍊接:https://www.nature.com/articles/s41593-023-01288-6